Questões sobre Termoquímica
Lista completa de Questões sobre Termoquímica para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Química - Termoquímica - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017

Em relação à termoquímica, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A máxima quantidade de energia que um sistema químico pode produzir é medida pela variação de energia livre: ΔG.
( ) Na entalpia da transformação, as medidas são geralmente efetuadas não mantendo uma pressão constante e é representada como ΔH.
( )Uma reação na qual o calor é absorvido (a temperatura da mistura de reação diminui quando reage) é chamada de endotérmica e o ΔH é positivo.
( )Uma reação na qual o calor é perdido pelos reagentes para o meio ambiente (a temperatura da mistura de reação aumenta quando reage) é dita exotérmica, onde ΔH é negativo.
A sequência está correta em
- A. V, V, F, F.
- B. V, F, V, V.
- C. F, V, F, V.
- D. F, F, V, V.
Acerca da termoquímica, da espontaneidade de reações e da ação de catalisadores, julgue os itens a seguir. Pela Lei de Hess, uma entalpia de reação é a soma das entalpias de qualquer sequência de reações, quando realizadas nas mesmas condições de temperatura e pressão, em que a reação total pode ser dividida.
- C. Certo
- E. Errado
A química é uma ciência que explica o mundo macroscópico por meio de modelos microscópicos com uma linguagem própria que representa as substâncias e suas transformações. A esse respeito, julgue os itens a seguir. A termoquímica permite calcular a energia liberada na forma de calor por uma reação, considerando-se valores de energia para ligações químicas.
- C. Certo
- E. Errado
A química é uma ciência que explica o mundo macroscópico por meio de modelos microscópicos com uma linguagem própria que representa as substâncias e suas transformações. A esse respeito, julgue os itens a seguir. A entalpia não informa se uma reação é espontânea ou não.
- C. Certo
- E. Errado
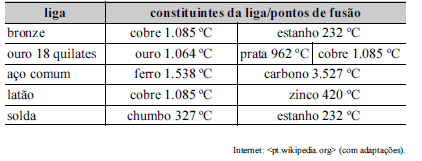
A partir dos dados na tabela precedente, relativos a ligas metálicas e pontos de fusão de seus constituintes, assinale a opção que apresenta a liga metálica que terá todos os seus componentes liquefeitos com o emprego de uma fonte de aquecimento a 450 ºC.
- A. ouro 18 quilates
- B. aço comum
- C. latão
- D. solda
- E. bronze
Sobre entalpia (H), assinale a afirmativa correta.
- A. A entalpia de um sistema é uma grandeza (expressa em unidades de energia) que informa a quantidade de energia desse sistema que poderia ser transformada em calor em um processo à temperatura constante.
- B. A entalpia de um sistema é uma grandeza (expressa em unidades de energia) que informa a quantidade de energia desse sistema que poderia ser transformada em calor em um processo à pressão constante.
- C. A entalpia de um sistema é uma grandeza (expressa em unidades de energia) que informa a quantidade de energia desse sistema que poderia ser transformada em calor em um processo a volume constante.
- D. A entalpia de um sistema é uma grandeza (expressa em unidades de energia) que informa a quantidade de energia desse sistema que poderia ser transformada em calor em um processo à pressão, volume e temperatura constantes.
Sobre as propriedades das substâncias puras e critérios de pureza, observe atentamente o gráfico abaixo. Considere que a amostra A apresenta estado físico inicial sólido à temperatura ambiente e 100% de pureza.
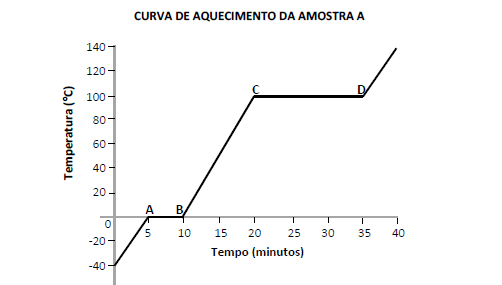
A partir dos dados do gráfico, marque V para as afirmativas verdadeiras e F para as falsas.
( ) No segmento AB, a amostra apresenta um patamar de ebulição.
( ) No segmento BC, a amostra encontra-se no estado líquido.
( ) Acima do ponto D, a amostra apresenta-se no estado de vapor.
( ) O segmento CD apresenta o patamar de fusão.
Assinale a sequência correta.
- A. V, F, F, V
- B. F, V, F, F
- C. V, F, V, V
- D. F, V, V, F
Foi realizado o desenvolvimento de um método cromatográfico para resolução e quantificação de componentes principais, de diferentes polaridades, em uma mistura complexa. O cromatograma A foi obtido em uma coluna apolar com o forno programado em modo isotérmico, a 45 oC. Modificações no método cromatográfico foram realizadas em sequencia, sendo obtidos os cromatogramas B e C.
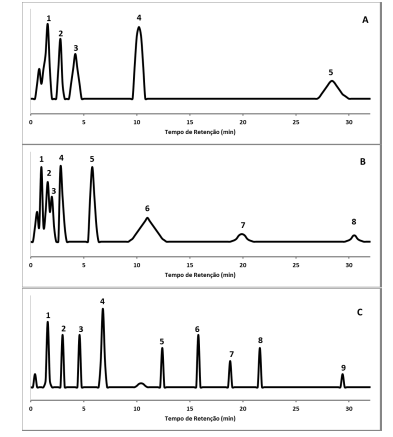
A sequência de modificações no método cromatográfico adotadas pelo analista para a obtenção dos cromatogramas B e C, partindo do cromatograma A, foram respectivamente:
- A. Diluição da amostra e adoção de uma coluna de maior polaridade.
- B. Aumento da temperatura do injetor e diminuição da temperatura do forno.
- C. Diminuição da temperatura do forno em modo isotérmico e adoção de uma coluna de maior polaridade.
- D. Aumento da temperatura do forno em modo isotérmico e aumento programado da temperatura da forno.
- E. Aumento programado da temperatura da forno e diminuição da temperatura do injetor.
O material pirofórico reage espontaneamente quando em contato com o oxigênio do ar, podendo inclusive reagir com a água. Essa capacidade de reação espontânea é influenciada pelo tamanho dos grãos do material. Com relação a esse assunto, julgue o item abaixo. O aumento da reatividade pela diminuição do tamanho das partículas está relacionado, entre outros fatores, ao aumento da área de contato superficial bem como à diminuição da capacidade de dissipação térmica dentro do próprio material piróforo.
- C. Certo
- E. Errado
Com relação à fabricação de cimento, julgue os seguintes itens. A reação química de calcinação do calcário ocorre em temperatura ambiente.
- C. Certo
- E. Errado


