Questões de Química da Fundação Getúlio Vargas (FGV)
Lista completa de Questões de Química da Fundação Getúlio Vargas (FGV) para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Os métodos de lavagem, descontaminação e desinfecção das vidrarias do laboratório devem considerar o contaminante, a utilização e o tipo da vidraria. Os processos de lavagem incluem solventes, detergentes especiais e água deionizada.
O processo de descontaminação das vidrarias utilizadas na cromatografia iônica deve incluir
- A. lavagem intensiva com detergente industrial.
- B. lavagem cuidadosa com água destilada.
- C. lavagem simplificada com ácido diluído.
- D. lavagem estimulada com mistura sulfocrômica.
- E. lavagem abundante com água deionizada.
Para preparar 100 mL de uma solução 0,20mol.L-1 de ácido clorídrico (a 20ºC) a partir do ácido concentrado (37% m/m e densidade 1,19 g.cm-3 a 20ºC), um técnico cumpriu as seguintes etapas:
I. Utilizando X tomou uma alíquota de 1,67 mL do ácido concentrado.
II. Transferiu para Y e completou o volume até 100 mL com água destilada.
As vidrarias apropriadas para o preparado da solução, representadas por X e Y, são, respectivamente,
- A. X proveta de 10 mL e Y proveta de 100 mL.
- B. X proveta de 5 mL e Y balão volumétrico de 100 mL.
- C. X pipeta graduada de 10 mL e Y proveta de 100 mL.
- D. X pipeta volumétrica de 2 mL e Y balão volumétrico de 1000 mL.
- E. X pipeta graduada de 2 mL e Y balão volumétrico de 100 mL.
Uma solução padrão em acetona de concentração 3,8x10-5 mol.L-1 de um carotenoide natural de fórmula molecular C40H56 apresentou absorvância 0,15 ua em comprimento de onda 503nm, em uma cubeta de caminho óptico de 1 cm.
Nessas mesmas condições de análise, uma amostra de concentração desconhecida do composto apresentou absorvância 0,10 ua.
Considerando que as amostras obedecem a lei de Lambert-Beer nas condições nas quais os espectros foram obtidos, a concentração da amostra desconhecida (em mg.L1) é aproximadamente igual a
Dados: Massas Molares (g.mol-1) H = 1, C = 12
- A. 2,5 x 104.
- B. 1,3 x 103.
- C. 3,8 x 102.
- D. 13,5.
- E. 1,7.
O mentol e a cânfora podem ser representados como
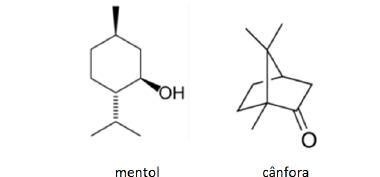
Essas substâncias estimulam os quimiorreceptores olfativos do cérebro e são utilizadas em alguns produtos por proporcionarem sensação de frescor.
As cadeias carbônicas do mentol e da cânfora
- A. são classificadas como saturadas.
- B. possuem o mesmo grupo funcional.
- C. apresentam a mesma fórmula molecular.
- D. possuem carbonos tetraédricos e lineares.
- E. possuem somente carbonos com hibridização sp3.
O carbeto de cálcio conhecido como carbureto quando adicionado à água produz o etino (acetileno) que é um gás utilizado em processos de soldagem (solda oxiacetilênica). A forma mais segura de se transportar o acetileno é através do carbureto (material sólido e mais estável)
A reação a seguir apresenta a reação do carbeto de cálcio e água:.

- A. 4880 L.
- B. 3360 L.
- C. 2240 L.
- D. 1220 L.
- E. 610 L.
Alguns parâmetros indicadores da qualidade da água são determinados por titulometria sendo necessária uma solução de concentração conhecida (solução padrão). Uma solução padrão é preparada diretamente a partir de uma substância de pureza conhecida (padrão primário) ou prepara-se uma solução de uma substância de pureza aproximada e determina-se sua concentração por titulação (padrão secundário).
Dentre as substâncias apresentadas a seguir, assinale aquela que pode ser utilizada como padrão primário.
- A. Hidróxido de sódio
- B. Nitrato de prata
- C. EDTA
- D. Permanganato de potássio
- E. Hidrogenoftalato de potássio
A determinação de oxigênio dissolvido em um determinado sistema aquático pode ser realizada por titulação (Método Winkler), que necessita do preparo de uma solução de tiossulfato de sódio conforme descrito a seguir. Em um béquer de 250 mL foi colocada uma determinada massa de tiossulfato de sódio (Na2S2O3) previamente pesada. O sal em questão foi dissolvido em 150 mL de água destilada. Essa solução foi cuidadosamente transferida para um balão volumétrico de 250,00 mL. O volume da solução foi completado com água destilada até a marca da aferição do balão que, posteriormente, foi tampado e agitado para completa homogeneização. Com esse procedimento foi preparada uma solução de tiossulfato de sódio de concentração 0,009mol.L1. A massa de Na2S2O3 necessária para o preparo dessa solução é:
- A. 0,158 g.
- B. 0,355 g.
- C. 0,112 g.
- D. 0,103 g.
- E. 0,071 g.
O tiocianato de ferro (III) dissolve-se facilmente em água dando origem a uma solução vermelha. A cor vermelha se deve à presença do íon FeSCN2+ hidratado.

Ao se adicionar pequena quantidade de tiocianato de sódio a essa solução em equilíbrio,
- A. ocorrerá a formação de um precipitado branco.
- B. a cor amarela da solução ficará mais intensa.
- C. a cor vermelha da solução ficará mais intensa.
- D. ocorrerá a formação de um precipitado marrom.
- E. a solução ficará incolor.
Na determinação da concentração de uma solução de ácido sulfúrico foi transferida uma alíquota de 25,00 mL da solução ácida para um erlenmeyer e posteriormente foram adicionadas 5 gotas de vermelho de metila. Com a utilização de uma bureta contendo uma solução 0,100 mol.L1 de hidróxido de sódio, a solução ácida foi titulada gastando-se nessa titulação 24,00 mL da solução alcalina.
O valor da concentração, em mol.L1, da solução de ácido sulfúrico é:
- A. 0,192.
- B. 0,096.
- C. 0,074.
- D. 0,048.
- E. 0,037.
Eletrodos de membranas íon-seletivos têm sido desenvolvidos, diferindo na composição física ou química da membrana. O mecanismo geral pelo qual o potencial íon-seletivo se desenvolve nesses dispositivos depende da natureza da membrana e está relacionado ao potencial de junção que se manifesta por meio de uma membrana que separa a solução do analito da solução de referência.
Assinale a opção que apresenta as características das membranas íon-seletivas.
- A. As membranas não devem exibir condutividade elétrica, ficando a medida elétrica restrita ao sistema eletroquímico a ser quantificado.
- B. As membranas agem seletivamente ao íon de interesse por meio de processos de troca iônica, cristalização ou complexação.
- C. As membranas são sensíveis aos íons e aos processos de transferência de elétrons que se manifestam em sua superfície.
- D. As membranas são insolúveis em meio eletrolítico, mas podem exibir solubilidade considerável em água pura.
- E. As membranas são sempre constituídas de vidro de silicato, com característica não cristalina.


