Questões sobre Geral
Lista completa de Questões sobre Geral para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
O Oxigênio é o elemento químico mais abundante na Terra com aproximadamente 44,8% da sua massa; Por isso, o gás oxigênio é fundamental para a manutenção da vida dos seres humanos, animais e plantas. O silício é o segundo elemento químico mais abundante com aproximadamente 27,7% da massa da Terra. Sabe se que o peso molecular da sílica é 60g/mol e do gás oxigênio é 32g/mol. A quantidade em matéria de oxigênio, é de aproximadamente:
- A. 1,9 vezes a quantidade de matéria do silício.
- B. 1,6 vezes a quantidade de matéria do silício.
- C. 2,7 vezes a quantidade de matéria do silício
- D. 1,1 vezes a quantidade de matéria do silício.
- E. Nenhuma das alternativas anteriores.
Analise as afirmativas a seguir com relação a segurança de laboratório de Biotecnologia.
I. Qualquer derramamento de substância que ocorrer no laboratório deverá ser imediatamente administrado, e medidas urgentes devem ser implementadas, a fim de evitar a perda de tempo e o controle da situação. Quanto à limpeza do material derramado, a mesma deverá ser realizada pelos próprios funcionários do laboratório. Para administrar a situação, é preciso que o funcionário seja devidamente capaz de identificar o tipo de material envolvido, decidir quais medidas deverão ser adotadas e proceder a limpeza, atendendo as normas de segurança, munido de todo o equipamento de proteção individual necessário, de modo a oferecer proteção aos olhos, mãos, pés, corpo e pulmões.
II. Os equipamentos de proteção individual devem estar disponíveis e em quantidade suficiente para dar a devida proteção aos funcionários do laboratório. A empresa é obrigada a disponibilizar todos os equipamentos necessários à proteção dos funcionários.
III. Planos de prevenção de incêndio devem ser implementados em todos os laboratórios, principalmente naqueles onde são utilizados materiais inflamáveis e/ou de fácil combustão. O fogo, quando gerado em ambientes de risco, pode levar a consequências de extrema gravidade, pois, nesses locais, o fogo se propaga com muita facilidade devido aos tipos de materiais que são inseridos e que são, na maioria das vezes, materiais combustíveis, substâncias inflamáveis e gases combustíveis.
IV. Quanto às práticas de laboratório que exigem equipamentos específicos, é preciso orientar profissionais dos mesmos a não lançar mão de improvisações com o intuito de agilizar as tarefas. Se houver necessidade de destilar qualquer solvente, certificar-se que a aparelhagem montada é compatível com a atividade e que o procedimento está sendo realizado em local próprio e com toda a segurança. Quando da destilação, o recomendado é o banho-maria. Jamais empregar chama direta.
V. Torna-se necessária a utilização de capelas de exaustão para manusear substâncias tóxicas e cabina de fluxo laminar para material biológico patogênico. Deve-se manter o vidro da capela abaixado o suficiente, de modo a ter somente as mãos inseridas no seu interior, sem jamais colocar a cabeça no interior da mesma.
Estão corretas:
- A. Apenas I, II e V
- B. Apenas II, III e IV
- C. Apenas II, III, IV e V
- D. Apenas I, IV e V
- E. I, II, III, IV e V
A estimativa da constante de Avogadro pode ser realizada através da eletrólise da água. Em um experimento que foi realizado por estudantes secundaristas para essa finalidade obteve-se 6,1x1023 como valor para a constante. Na realização desse experimento, foram empregados fios de cobre de 2,5mm de diâmetro, duas seringas de injeção de 10,0mL, um pedaço de isopor para servir com suporte para as seringas, solução de hidróxido de sódio 10g/L, bateria de 6V e uma cuba de plástico. Através de um amperímetro, mediu-se a corrente que saiu da fonte cujo valor foi de 30mA. O experimento foi montado conforme a ilustração, Figura 1. Considerando a pressão local igual a 663mmHg, R = 8,314 J/Kmol, a temperatura ambiente de 27ºC e o volume de Hidrogênio coletado de 5,5 mL, em quanto tempo, aproximadamente, ocorreu o experimento:
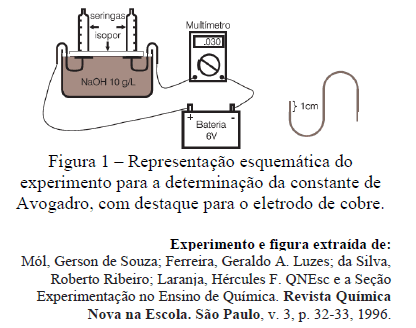
- A. 205s
- B. 1306s
- C. 893s
- D. 1427s
- E. 155s
Um reator de pirólise, em escala de laboratório, é usado para a produção de bio-óleo e carvão durante o aproveitamento energético de biomassa residual, operando a uma vazão mássica de 0,5 kg/hora. Considerando os dados abaixo, podemos informar que os rendimentos dos produtos, carvão e óleo (respectivamente), após 30 minutos de operação do sistema, são aproximadamente:
Dados:
- Massa de carvão obtida no processo = 125 g
- Volume de bio-óleo recuperado = 70 mL
- Densidade do bio-óleo = 1,1 g/mL
- A. 50 e 31%
- B. 40 e 20 %
- C. 50 e 25 %
- D. 45 e 19 %
- E. 30 e 20 %
A produção de energia elétrica a partir da biomassa, atualmente, é muito defendida como uma alternativa importante para países em desenvolvimento e também outros países. Programas nacionais começaram a ser desenvolvidos visando o incremento da eficiência de sistemas para a combustão, gaseificação e pirólise da biomassa. Com relação às principais tecnologias de aproveitamento de biomassa, podemos afirmar, exceto:
- A. A combustão é um processo de transformação da energia química dos combustíveis em calor, por meio das reações dos elementos constituintes com o oxigênio fornecido. Ocorre em fornos (metalurgia, por exemplo) e caldeiras (geração de vapor, por exemplo).
- B. A transesterificação é um processo químico que consiste na reação de óleos e gorduras com um produto intermediário ativo (metóxido ou etóxido), oriundo da reação entre álcoois (metanol ou etanol) e uma base (hidróxido de sódio ou de potássio).
- C. O processo de biodigestão consiste na decomposição do material pela ação de microrganismos (bactérias acidogênicas e metanogênicas). Trata-se de um processo simples, que ocorre naturalmente com quase todos os compostos orgânicos, com formação de biogás. O processo ocorre em condições aeróbias e anaeróbias.
- D. A pirólise é um processo que consiste em aquecer o material original (normalmente entre 300°C e 500°C), na quase ausência de ar, até que o material volátil seja retirado. O principal produto final (carvão) tem uma densidade energética bem maior que aquela do material de origem. Além de carvão, o processo produz bio-óleo, extrato ácido e gases combustíveis.
- E. O processo de cogeração é a geração simultânea de energia térmica e mecânica, a partir de uma mesma fonte primária de energia. As formas de energia útil mais frequente são a energia mecânica (movimentar máquinas, equipamentos e turbinas de geração de energia elétrica) e a térmica (geração de vapor, frio ou calor).
Os alimentos são produtos de composição química complexa que, em estado natural, processados ou cozidos, são consumidos pelo homem como fonte de nutrientes para a sua satisfação sensorial. Com relação à química dos alimentos, podemos afirmar, exceto:
- A. A estrutura dos lipídeos pode ser modificada mediante a aplicação de certos tratamentos (hidrogenação, transesterificação e fracionamento), que implicam mudanças nas características físicas de uma gordura ou de um óleo.
- B. As proteínas são componentes importantes dos alimentos que influem diretamente em suas características sensoriais e, portanto, em sua aceitabilidade. Os alimentos de origem animal possuem grande conteúdo em proteínas, o que lhes confere alto valor nutritivo.
- C. Os carboidratos constituem a principal fonte de energia da dieta, contribuindo também para que os alimentos sejam mais apetecíveis e de aspecto mais agradável. Durante os tratamentos térmicos dos alimentos, os carboidratos podem sofrer transformações como escurecimento não-enzimático e caramelização.
- D. A capacidade de estabelecer ligações de hidrogênio e a polaridade da molécula de água fazem dela um grande solvente, tanto para compostos iônicos como não-iônicos de caráter polar. A água não atua na dispersão de compostos que contêm grupos apolares ou hidrófobos.
- E. Nas operações de lavagem, branqueamento e cocção em água, sempre há perdas de vitaminas hidrossolúveis e, sobretudo, de minerais por lixiviação. A intensidade dessas perdas está relacionada com: pH do meio, temperatura , quantidade de água no alimento e superfície do alimento exposta á água.
Um tanque em forma de cilindro circular reto está sendo alimentado com óleo combustível à razão de 4 m3/min. Sabendo-se que o diâmetro do cilindro vale 5 m, podemos estimar que a altura do combustível está aumentando a uma razão de:
- A. 4/(25
 ) m/min
) m/min - B. 4/(6,25
 ) m/min
) m/min - C. 4/(5
 ) m/min
) m/min - D. 4/(20
 ) m/min
) m/min - E. 5/(4
 ) m/min
) m/min
Uma amostra de calcário (CaCO3), cuja pureza era de 60%, foi empregada na produção da CAL, através da decomposição térmica do material a 850 oC. Decompondo-se 500 kg de massa dessa amostra, obteve-se cal virgem (CaO) e gás carbônico (CO2). Admitindo-se um rendimento de 70% para essa reação, a quantidade de quilos de cal virgem obtida, vale: (Considerar: C = 12 ; O = 16 ; Ca = 40.)
- A. 168 kg
- B. 300 kg
- C. 250 kg
- D. 117,6 kg
- E. 150, 2 kg
Foram estudados através de planejamento fatorial do tipo 22 os efeitos da temperatura e catalisador sobre o rendimento de uma reação química. Os dados experimentais obtidos são apresentados na tabela a seguir. Nos ensaios foram empregados dois níveis para a temperatura (40 e 50 oC) e dois tipos de catalisadores (A e B). Cada ensaio foi feito em duplicata.
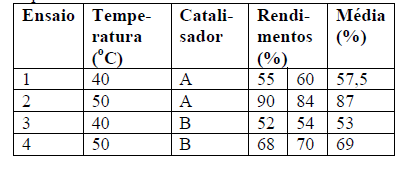
Analise as afirmativas a seguir com relação aos dados experimentais obtidos durante os ensaios.
I. Quando usamos o catalisador A e aumentamos a temperatura de 40 para 50 oC (ensaios 1 e 2), o rendimento médio aumenta em 29,5 %.
II. Quando usamos o catalisador B e modificamos a temperatura de 40 para 50 oC (ensaios 3 e 4), o rendimento médio aumenta em 16 %.
III. A 50 oC (ensaios 2 e 4) a mudança do tipo de catalisador diminui o rendimento médio da reação em 18 %. IV. Não existe efeito de interação entre as variáveis estudadas (temperatura e tipo de catalisador) nesse planejamento experimental.
V. Elevando a temperatura, aumentamos o rendimento da reação, mas esse efeito é muito mais pronunciado com o catalisador B do que com o catalisador A.
Estão corretas:
- A. I, II e V
- B. II, III e IV
- C. II, III, IV e V
- D. I, IV e V
- E. I, II e III
A cromatografia pode ser combinada a diferentes sistemas de detecção, tratando-se de uma das técnicas analíticas mais utilizadas e de melhor desempenho. O acoplamento de um cromatógrafo com o espectrômetro de massas combina as vantagens da cromatografia (alta seletividade e eficiência de separação) com as vantagens da espectrometria de massas (obtenção de informação estrutural, massa molar e aumento adicional da seletividade). Observe as informações a seguir:
I. O método de impacto de elétrons é a técnica mais usada de geração de íons para a espectrometria de massas. As moléculas de amostra são bombardeadas na fase de gás com elétrons de alta energia. Em algumas situações, ocorre a remoção de um elétron da molécula da amostra para produzir um cátion-radical, conhecido como o íon molecular.
II. No processo de ionização por impacto de elétrons sempre gera o íon molecular do composto químico da amostra analisada.
III. A espectrometria de massas com ionização química é útil para a comparação de picos no espectro de massas. Seu principal uso é para se verificar a quantidade de íons formados durante a análise.
IV. O analisador de massas separa a mistura de íons formados durante a etapa de ionização segundo seus m/z (razão massa/carga) para a geração de um espectro de massas.
V. Na técnica de impacto de elétrons, o espectrômetro de massas bombardeia com um feite de elétrons de alta energia as moléculas que estão na fase de vapor e registra o espectro dos íons positivos, depois de separados na base da razão massa /carga.
Com relação á cromatografia com detecção através de espectrometria de massas, são verdadeiras as informações:
- A. I, IV e V
- B. I, II e V
- C. II, III e IV
- D. II, III, IV e V
- E. I, II, III, IV e V


