Questões de Engenharia Química
Lista completa de Questões de Engenharia Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
Em um laboratório de análise química, há três tambores plásticos (X, Y e Z) destinados ao descarte de soluções e nos seus rótulos se lê os seguintes dizeres:

Considerando que o correto descarte tenha sido feito pelo perito, assinale a alternativa correta.
- A. A solução 3 foi descartada no tambor Y já que, em solução, a glicose apresenta caráter alcalino.
- B. A solução 2 foi descartada no tambor X, pois a solução de hidróxido de sódio, no volume e na concentração empregados, não eram capazes de neutralizar completamente a solução de ácido clorídrico.
- C. As três soluções foram descartadas no tambor Z já que todas apresentam pH=7.
- D. Por ser proveniente de base forte, a solução 1 foi descartada no tambor Y.
- E. A solução 2 poderia ser corretamente descartada no tambor Z se tivesse sido preparada a partir de 50 mL de ácido clorídrico de concentração 0,1 mol/L adicionado a 20 mL de uma solução aquosa hidróxido de sódio, de concentração 0,5 mol/L.
 Considerando o que foi apresentado, assinale a alternativa correta.
Considerando o que foi apresentado, assinale a alternativa correta.
- A. A massa de cocaína contida em 5.000 tubos era de 225g.
- B. A densidade do pó contido em cada tubo era de 0,33 g/mL.
- C. A massa da totalidade dos tubos (10.000 tubos), após a remoção da totalidade do pó, era de 5.000g.
- D. A massa de pó apreendida que não correspondia à cocaína era de 4.750g.
- E. A densidade do pó contido em cada tubo era de 1,0 g/mL.
 A quantidade de cocaína presente em um único tubo era de:
A quantidade de cocaína presente em um único tubo era de:
- A. 2,5 mg.
- B. 5,0 mg.
- C. 25 mg.
- D. 50 mg.
- E. 500 mg.
Zezinho é um perito que foi encarregado de analisar, por meio de cromatografia gasosa acoplada à espectrometria de massas (com ionização por impacto de elétrons), um lote de padrões analíticos das moléculas abaixo listadas:
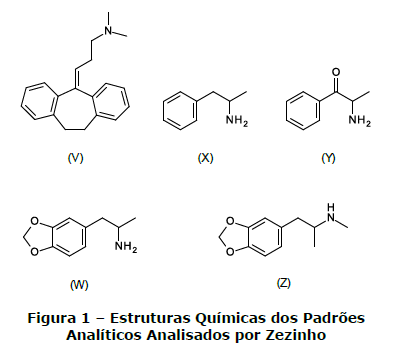
No entanto, antes das análises e na tentativa de prever qual seria o perfil de fragmentação de cada uma dessas moléculas, Zezinho formulou cinco hipóteses, dentre as quais, assinale a única que se mostrará correta.
- A. As moléculas V, X e Z apresentarão em comum um fragmento com m/z = 58, originário de fragmentação comumente observada em aminas.
- B. As moléculas X e Y apresentarão um mesmo fragmento de m/z = 44, originário de fragmentação comumente observada em aminas.
- C. As moléculas W e Z, por se tratarem de isômeros de posição, apresentarão espectros semelhantes.
- D. A molécula Z não apresentará fragmento com m/z que possa ser encontrado em pelo menos uma das demais estruturas analisadas.
- E. Todas as aminas primárias analisadas apresentarão um fragmento comum de m/z = 58.
Álcoois são de grande versatilidade do ponto de vista sintético, pois podem participar de uma série de reações. Exemplos dessa versatilidade são mostrados nas reações não balanceadas nas quais apenas o produto principal é mostrado:
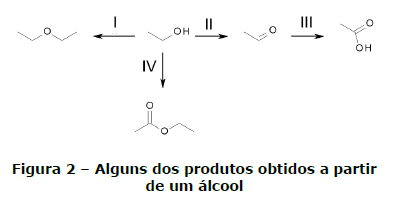
Sobre essa reação e os compostos nela envolvidos, assinale a alternativa INCORRETA.
- A. Em I ocorre uma desidratação intermolecular. Se essa desidratação fosse intramolecular, o produto seria um alceno.
- B. Os produtos das reações I e IV são mais apolares do que os reagentes.
- C. Os produtos das reações de oxidação II e III apresentam carbono sp2 e carbono sp3.
- D. O produto da reação III, quando adicionado à água com pOH maior do que 7, encontrarse- á mais ionizado do que em água com pOH menor do que 7.
- E. A combustão completa tanto do reagente quanto dos produtos mostrados em I, II, III e IV formará gás carbônico e água.
Considerando a reação de combustão do metano (CH4(g)), é correto afirmar que se trata de um processo termoquímico:
- A. Endotérmico, com liberação de energia e ΔH<0.
- B. Exotérmico, com liberação de energia e ΔH<0.
- C. Exotérmico, com liberação de energia e ΔH >0.
- D. Endotérmico, com absorção de energia e ΔH>0.
- E. Exotérmico, com absorção de energia e ΔH<0.
Considere os seguintes tipos de materiais vegetais:
Folhas de coca (Erythroxylum coca), das quais se extraem o alcalóide cocaína (observação: comporta-se como base fraca).
Folhas de maconha (Cannabis sativa) das quais se obtém diferentes canabinóides, dentre os quais, o delta-9 tetraidrocanabinol (delta-9 THC), molécula de baixa hidrossolubilidade.
Para a extração dos princípios ativos desses materiais vegetais, um laboratório forense dispõe dos seguintes sistemas de solventes para extração:
I. Clorofórmio acrescido de ácido acético glacial (H3C-COOH).
II. Clorofórmio (CHCl3) acrescido de hidróxido de amônio.
III. Clorofórmio puro (CHCl3).
IV. Tolueno (hidrocarboneto aromático de fórmula: C7H8). V. Solução aquosa 10-5 mol/L de ácido clorídrico.
VI. Solução aquosa 10-5 mol/L de hidróxido de sódio.
VII. Água pura.
Considerando que os sistemas de solventes já foram exaustivamente testados e que não causarão degradação dos princípios ativos e que os protocolos de extração do laboratório preveem o uso sempre da mesma quantidade de material vegetal e de solventes (todos em temperatura ambiente) para todas as metodologias de extração, assinale a alternativa INCORRETA.
- A. A extração das folhas de coca com o sistema VII será mais efetiva do que com o sistema V.
- B. A extração da cocaína será mais eficiente com o sistema II do que com I.
- C. O sistema IV é recomendado para a extração de delta 9-THC já que este apresenta baixa polaridade, tal qual o tolueno.
- D. Ao usar o sistema I, a cocaína estará em uma forma mais polar do que estaria se o sistema empregado fosse o II.
- E. Dentre os sistemas disponíveis no laboratório, não são os mais recomendados para extração do delta-9-THC: V, VI e VII.
Um perito resolveu usar o cloreto de etila (I) como modelo de estrutura química para testar um software de previsão de espectros de Ressonância Magnética Nuclear de 1H. A partir dessa molécula, foram feitas substituições que originaram outros compostos similares (II, III, IV, V e VI), que também foram testados.
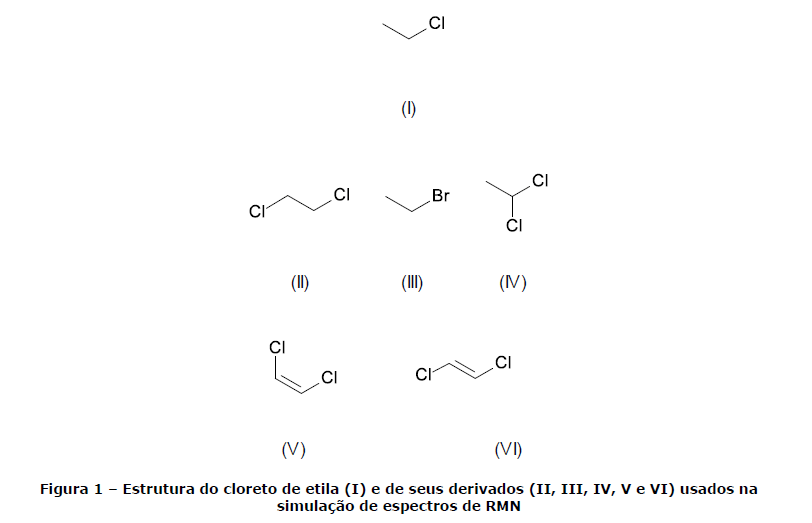
Os testes do software não incluíam sobreposição de espectros de solventes, nem de agentes como o TMS. Considerando as moléculas e as observações teóricas feitas pelo perito, assinale a alternativa INCORRETA.
- A. O espectro observado do cloreto de etila (I) apresentava um quarteto e um tripleto.
- B. Ao substituir um dos átomos de hidrogênio do carbono inicialmente não halogenado por um átomo de cloro (II), o perito observou um singleto.
- C. Ao trocar o átomo de cloro na molécula do cloreto de etila (I) por um de bromo (formando III), o perito observou que o sinal referente aos hidrogênios do carbono halogenado se deslocou no sentido do campo mais alto.
- D. A substituição de um dos átomos de hidrogênio do carbono inicialmente halogenado por um átomo de cloro (originando IV) fez com que o perito observasse um dubleto e um quarteto.
- E. A partir do cloreto de etila, a introdução de uma dupla ligação entre os átomos de carbono e a substituição de um dos átomos de hidrogênio do carbono não halogenado por cloro poderia originar dois isômeros: um cis (V) e outro trans (VI), cujos espectros apresentaram multiplicidades diferentes.
Em relação a um ciclo consistindo em uma pressão constante, um volume constante e dois processos isentrópicos, analise as assertivas abaixo:
I. Ciclo de Carnot.
II. Ciclo de Stirling.
III. Ciclo Otto.
IV. Ciclo Diesel.
Quais estão corretas?
- A. Apenas I.
- B. Apenas IV.
- C. Apenas II e III.
- D. Apenas I, II e III.
- E. I, II, III e IV.
Qual das seguintes medidas aumentará o volume de um gás real por quatro vezes?
- A. Duplicando a temperatura absoluta, bem como a pressão do gás.
- B. Duplicando a pressão absoluta, mas não alterando a temperatura.
- C. Reduzindo a pressão para um quarto à temperatura constante.
- D. Reduzindo a temperatura para um quarto à pressão constante.
- E. Reduzindo a temperatura para metade e dobrando a pressão.


