Questões de Química
Lista completa de Questões de Química para resolução totalmente grátis. Selecione os assuntos no filtro de questões e comece a resolver exercícios.
A aferição de soluções volumétricas é uma prática comum em laboratório. O hidróxido de sódio (NaOH) é um reagente padrão secundário, portanto, as soluções volumétricas preparadas a partir desse reagente devem ser aferidas. Durante a aferição em duplicata de uma solução 0,5 mol/L de NaOH frente o reagente biftalato de potássio (C8H5KO4), obteve-se os seguintes resultados:

- A. 1,000
- B. 0,971
- C. 1,029
- D. 0,948
- E. 1,055
Química - Elementos Químicos, Substâncias e propriedades químicas, Tabela Periódica - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
Embora os gases sejam simples, tanto de descrever quanto em termos de sua estrutura interna, eles são de imensa importância. Nós passamos toda a nossa vida envolvidos por um gás na forma de ar e a variação local nas suas propriedades é o que nós chamamos de tempo. Sobre os gases, é INCORRETO afirmar que: (Considere: ln 0,50 = 0,69.)
- A. A velocidade média quadrática das moléculas num gás é proporcional à raiz quadrada da temperatura.
- B. A razão entre as velocidades com que o hidrogênio e o dióxido de carbono se efundem nas mesmas condições de pressão e a temperatura é 4,69.
- C. A seção eficaz de colisão do O2 é 0,40. O livre percurso médio das moléculas de O2 numa amostra de oxigênio nas CNATP (25°C, 1 bar) é 3,7 x 108 m.
- D. Admitindo que a pressão parcial de um gás perfeito caia de 1,00 bar a 0,50 bar, quando o gás é consumido numa reação a 25°C, a variação do potencial químico é 1,7 kJ/mol.
Deseja-se preparar 500 mL de uma solução de ácido clorídrico (HCl) 0,1 mol/L a partir do reagente PA. Qual deverá ser o volume de HCl utilizado no preparo da solução?
Dados: Massa molar HCl: 36,46 g/mol
Densidade do reagente HCl PA: 1,19 kg/L
Pureza do reagente HCl PA: 37% m/m
- A. 1,53 mL
- B. 4,93 mL
- C. 1,82 mL
- D. 3,64 mL
- E. 4,14 mL
Química - Termoquímica - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
A lei que é usada para identificar o sentido da mudança espontânea, a segunda lei da termodinâmica, também se exprime em termos de uma função de estado, a entropia. A primeira lei usa a energia interna para identificar as mudanças permitidas; a segunda lei usa a entropia para identificar as mudanças espontâneas entre as mudanças permitidas.
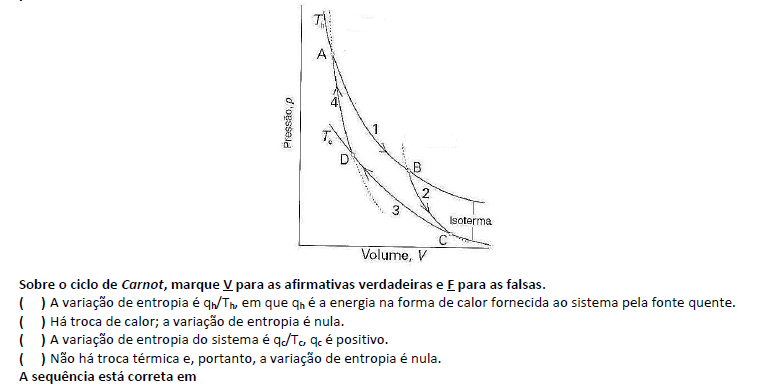
- A. F, F, V, V.
- B. V, F, F, V.
- C. V, V, F, F.
- D. F, V, F, V.
A solução de ácido bórico (H3BO3) 4,0% m/v é utilizada durante a etapa de destilação da análise de determinação do nitrogênio pelo método de Kjeldahl . Qual é o volume de solução 1 mol/L de H3BO3 que deve ser adicionado a 200 mL de solução de H3BO3 2,0% m/v para obter a solução desejada de H3BO3 4,0% m/v?
Dado: Massa molar H3BO3: 62,83 g/mol
- A. 17,52 mL
- B. 375,21 mL
- C. 175,21 mL
- D. 37,52 mL
- E. 75,04 mL
Química - Reações, Soluções e Transformações Químicas - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
Reações de oxidação e redução podem ocorrer em muitos sistemas químicos. Exemplos incluem nosso próprio sistema respiratório e o sistema fotossintético complementar nas plantas. Além disso, podemos pensar no processo de assar o pão, no enferrujamento do ferro, na ação dos alvejantes sobre as manchas e na produção e combustão do petróleo. Nesse contexto, analise as afirmativas a seguir.
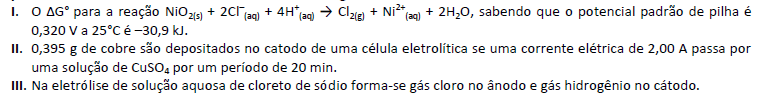
Está(ão) correta(s) apenas a(s) afirmativa(s)
- A. III.
- B. I e II.
- C. I e III.
- D. II e III.
Química - Sistemas de equilíbrio - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
A ebulição, o congelamento e a conversão da grafita em diamante são exemplos de transições de fase, ou mudanças de fase sem mudança de composição química. Muitas mudanças de fase são fenômenos cotidianos comuns e a sua descrição é importante. Elas ocorrem quando um sólido se transforma num líquido, como na fusão do gelo, ou um líquido se transforma num vapor, como na vaporização da água em nossos pulmões. Sobre as transformações físicas, analise as afirmativas a seguir.
I. O hélio tem comportamento pouco comum nas temperaturas baixas. As fases sólida e vapor nunca estão em equilíbrio. O hélio sólido pode ser obtido, mas somente quando os átomos são forçados a se manterem juntos pela aplicação de uma pressão externa.
II. No equilíbrio, o potencial químico de uma substância é o mesmo em toda a amostra, qualquer que seja o número de fases presentes.
III. Uma diminuição de pressão eleva o potencial químico de qualquer substância pura, pois Vm > 0.
Está(ão) correta(s) apenas a(s) afirmativa(s)
- A. III.
- B. I e II.
- C. I e III.
- D. II e III.
Química - Química Inorgânica - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
Os polímeros ou plásticos, como são mais conhecidos são uma classe de materiais dos quais a sociedade do século XXI é bastante dependente. O emprego de materiais poliméricos na vida diária é cada vez mais significativo. Pode-se facilmente comprovar isso observando os inúmeros materiais que são fabricados utilizando compostos poliméricos, como, por exemplo, tubos de encanamento, canetas, sacos de lixo, roupas, eletrodomésticos etc. Sobre os polímeros, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Na polimerização de condensação, os monômeros não precisam apresentar ligação dupla entre carbonos, mas é necessária a existência de dois tipos de grupos funcionais nos dois monômeros diferentes.
( ) Tem-se como exemplo de polímeros lineares e ramificados o nylon, polietileno, policloreto de vinila e poliestireno.
( ) Policloreto de vinila é um polímero de condensação, termoplástico de rigidez elevada e excelente resistência química.
( ) O poliuretano é um elastômero. Após a vulcanização, o material é termofixo, possui baixa elasticidade e alta resistência à abrasão.
A sequência está correta em
- A. F, F, V, V.
- B. V, F, F, V.
- C. V, V, F, F.
- D. F, V, F, V.
Química - Eletroquímica - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
Pilha de aeração diferencial é a pilha constituída de eletrodos de um só material metálico em contato com um mesmo eletrólito, mas apresentando regiões com diferentes teores de gases dissolvidos. Como ocorre com mais frequência em regiões diferentemente aeradas, é conhecida como o nome de pilha de aeração diferencial. (Considere: potencial padrão de redução é E° = 0,401 V.)
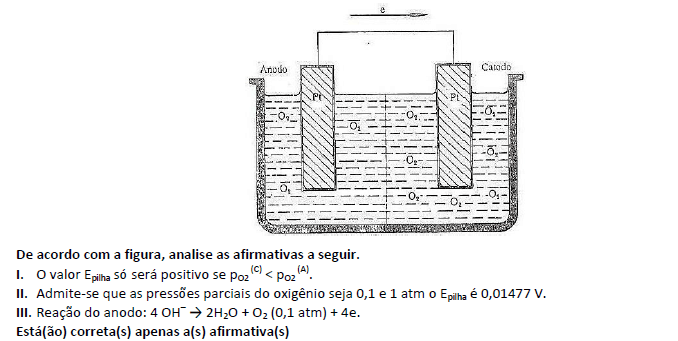
- A. III.
- B. I e II.
- C. I e III.
- D. II e III.
Química - Termoquímica - Intituto de Desenvolvimento Educacional, Cultural e Assistencial Nacional (IDECAN) - 2017
Um gás ideal com volume inicial de 6 litros sofreu uma transformação isotérmica e teve sua pressão reduzida para 40% de seu valor inicial. Nessa transformação, o gás apresentou um aumento no seu volume correspondente a:
- A. 4 litros.
- B. 5 litros.
- C. 9 litros.
- D. 10 litros.


